
 Foto: Hospital São Francisco
Foto: Hospital São Francisco Em 18 anos, o excesso de peso da população brasileira aumentou em 20 pontos percentuais. Em 2024, 62,6% dos brasileiros tinham excesso de peso, contra 42,6% em 2006. A obesidade (IMC igual ou maior que 30 kg/m²) dobrou, passando de 11,8% para 25,7% da população.
Os dados são do Sistema de Vigilância de Fatores de Risco e Proteção para Doenças Crônicas por Inquérito Telefônico (Vigitel) do Ministério da Saúde, divulgados nesta quarta-feira (28). O levantamento é realizado em todas as capitais e no Distrito Federal.
O diagnóstico médico de diabetes em adultos apresentou aumento de 5,5%, em 2006, para 12,9% em 2024. A hipertensão em adultos passou de 22,6% para 29,7%.
A atividade física no deslocamento pelas cidades diminuiu de 17% em 2009 para 11,3% em 2024 devido ao maior uso de carros por aplicativos e transporte público. Já a atividade moderada no tempo livre com pelo menos 150 minutos semanais cresceu de 30,3% em 2009 para 42,3% em 2024.
O consumo regular de frutas e hortaliças (5 dias por semana ou mais) manteve-se relativamente estável, variando de 33% (2008) para 31,4% (2024).
O consumo de refrigerantes e sucos artificiais (5 dias por semana ou mais) teve redução de 30,9% (2007) para 16,2% (2024).
O ministro da Saúde, Alexandre Padilha, avaliou que dados positivos como diminuição do consumo de refrigerante e aumento da atividade física não têm sido suficientes para reduzir a incidência de doenças crônicas como diabetes, hipertensão e obesidade.
“À medida que o Brasil vai envelhecendo cada vez mais, surgem mais pessoas com doenças crônicas. Por isso, precisamos ter mais políticas de cuidado e prevenção”, defendeu.
 Foto: Marcelo Camargo/Agência Brasil
Foto: Marcelo Camargo/Agência Brasil A Anvisa formou maioria nesta quarta-feira (28) para permitir o cultivo de novas de cannabis medicinal no Brasil. As informações são do G1.
A medida permite que a planta seja produzida no país para abastecer a fabricação de medicamentos e outros produtos regulados pela agência.
Até então, mesmo com a autorização para manipulação, registro e comercialização, o cultivo da cannabis no Brasil era proibido para a indústria, o que obrigava as empresas a importar a planta ou seus extratos. Essa restrição também limitava o avanço da pesquisa científica no país.
A mudança na regra segue um pedido Superior Tribunal de Justiça (STJ). Em novembro de 2024, o tribunal determinou que a Anvisa regulamentasse o cultivo da planta, desde que exclusivamente para fins medicinais e farmacológicos.
A permissão é um passo importante, segundo especialistas, para a mudança e ampliação do mercado de cannabis de medicinal no país.
Hoje, apenas produtos são permitidos -- o que é diferente de medicamentos. Eles têm menores concentrações, não passam por pesquisas de eficácia.
Para que um medicamento seja desenvolvido e registrado, é necessário um processo amplo de pesquisa -- o que ficava comprometido pela ausência de autorização para o cultivo da planta no Brasil. Agora, a expectativa é da consolidação de um mercado nacional de medicamentos.
 Foto: Freepik
Foto: Freepik A Agência Nacional de Vigilância Sanitária (Anvisa) determinou a apreensão e proibição da comercialização, distribuição e uso das fitas de clareamento dental “9D White Teeth Whitening Strips” em todo o Brasil.
A medida foi tomada após constatar que o produto não possuía registro na agência e que a empresa responsável, VM Global Trade Ltda., não tinha autorização para atuar no setor de saúde. A decisão foi formalizada pela Resolução-RE nº 306, publicada no Diário Oficial da União.
O 9D White Teeth Whitening Strips é um produto importado que não passou pela avaliação da Anvisa, portanto, não foi submetido a testes de segurança, eficácia e qualidade.
Isso significa que não há garantias de que o produto seja seguro para uso, o que representa um risco potencial à saúde dos consumidores. A Anvisa destacou que o uso de produtos sem registro pode causar danos à saúde bucal e geral, como sensibilidade nos dentes, irritação gengival e até desgaste do esmalte dental.
A Anvisa reforçou que a proibição da fita inclui a suspensão de suas atividades comerciais, de importação e propaganda. Além disso, a agência determinou a apreensão dos lotes do produto já disponíveis no mercado, evitando que mais consumidores sejam expostos a possíveis riscos.
 Foto: Isaque Pascoal/Sesab
Foto: Isaque Pascoal/Sesab A Bahia avançou no fortalecimento da atenção oncológica no Sistema Único de Saúde (SUS) com a implementação do Componente da Assistência Farmacêutica em Oncologia (AF-Onco). A iniciativa reafirmou o compromisso do Governo do Estado com a qualificação da gestão e com a garantia do cuidado integral às pessoas com câncer.
Instituído pela Portaria GM/MS nº 8.477, o AF-Onco aprimorou a organização do acesso a medicamentos oncológicos no país ao qualificar os processos de aquisição, distribuição e dispensação de fármacos, incluindo medicamentos orais e terapias inovadoras. O componente consolidou a Assistência Farmacêutica como eixo estratégico da política oncológica, ao estabelecer diretrizes claras para o financiamento e a aquisição de medicamentos, com responsabilidades compartilhadas entre União, estados e municípios, especialmente no que se refere aos medicamentos de alto custo.
Entre os avanços promovidos pelo AF-Onco destacou-se a integração dos medicamentos oncológicos à Relação Nacional de Medicamentos Essenciais (Rename), reforçando a padronização da oferta no SUS e ampliando a equidade no acesso às terapias em todo o território nacional. O modelo previu três modalidades de aquisição: compra centralizada pelo Ministério da Saúde; negociação nacional coordenada pela União, com execução pelos estados; e aquisição descentralizada, sob responsabilidade de estados e municípios, para medicamentos de menor complexidade.
A Secretaria da Saúde do Estado da Bahia (Sesab) participou do II Workshop Nacional de Gestão da Assistência Farmacêutica em Oncologia no SUS, que reuniu gestores estaduais, técnicos, especialistas e representantes de instituições estratégicas. Ao longo dos dois dias de programação, foram debatidos aspectos relacionados à articulação interfederativa, à integração entre áreas técnicas das secretarias estaduais de saúde e ao fortalecimento da governança da Assistência Farmacêutica em Oncologia.
 Foto: Fernando Munareto
Foto: Fernando Munareto Neste ano de 2026, alguns eventos climáticos poderão impactar o dia a dia no planeta Terra.
Ao site Achei Sudoeste e ao Programa Achei Sudoeste no Ar, Fernando Munareto, presidente da Associação dos Astrônomos Amadores da Bahia (AAAB), informou que o pico de atividade solar, que é registrado a cada 11 anos, terá repercussões na vida das pessoas.
Munareto explicou que, a cada 11 anos, o sol passa por períodos de baixa e alta atividade solar, que estão associados à quantidade de manchas solares em sua superfície. Ao longo de um ciclo solar, o sol passará de um período calmo para um período intenso e ativo.
Durante o pico de atividade, chamado de máximo solar, os polos magnéticos do sol se invertem. Então, o sol ficará quieto novamente durante um mínimo solar. “É um fenômeno que a gente ainda tenta estudar e compreender. Começou a ser observado no século XVII. Quando o sol entra nesse pico de atividade, ele começa a ter muitas explosões e manchas. Isso caracteriza esses picos de atividades. Esse ano está sendo assim”, relatou.
Segundo o especialista, o fluxo de vento solar lançado em direção à Terra nesse período em quantidade maior que o normal causará uma tempestade magnética nos próximos dias.
Os sistemas de comunicação via satélite poderão ser afetados. “A grande população não sente porque a maioria da internet é distribuída por fibra ótica, mas as empresas de comunicação normalmente têm prejuízos de milhões quando acontece esse tipo de fenômeno”, afirmou.
Os picos solares também aumentam a incidência de câncer de pele, exigindo maior proteção no período.
 Foto: Marcelo Camargo/Agência Brasil
Foto: Marcelo Camargo/Agência Brasil Os medicamentos à base de tirzepatida das marcas Synedica e TG, e de retatrutida, de todas as marcas e lotes, tiveram sua comercialização, distribuição, fabricação, importação, divulgação e uso proibidos pela Agência Nacional de Saúde (Anvisa) nesta quarta-feira (21). Esses produtos são popularmente conhecidos como “canetas emagrecedoras do Paraguai”.
Segundo a agência, esses medicamentos são produzidos por empresas desconhecidas e são vendidos – em perfis no Instagram – “sem registro, notificação ou cadastro na Anvisa”.
A Anvisa diz também em seu comunicado que, por serem irregulares e de origem desconhecida, “não há garantia sobre o seu conteúdo ou qualidade”, e que por isso essas canetas emagrecedoras não podem ser usadas “em nenhuma hipótese”.
A resolução sobre a proibição foi publicada no Diário Oficial da União nesta quarta.
 Foto: Divulgação
Foto: Divulgação Um projeto de lei que garante o fornecimento de medicamentos para pessoas com transtorno do espectro autista (TEA) no Sistema Único de Saúde (SUS) foi aprovado pela Comissão de Saúde da Câmara dos Deputados.
O texto aprovado é um substitutivo do relator, deputado Amom Mandel (Cidadania-AM), ao projeto do deputado Saullo Vianna (União-AM), que previa que o SUS deveria fornecer qualquer medicamento prescrito por um médico, da rede pública ou privada. No entanto, o relator argumentou que a medida seria inviável por obrigar o SUS a fornecer medicamentos sem registro na Agência Nacional de Vigilância Sanitária (Anvisa) para esse fim — uso off-label — o que contraria a legislação.
“Propomos assegurar aos pacientes com TEA o fornecimento de medicação por meio da elaboração de protocolo clínico e diretrizes terapêuticas para tratamento das comorbidades e dos seus sintomas mais frequentes, conforme as melhores evidências científicas disponíveis”, afirmou o relator, que disse que a proposta original poderia obrigar o SUS a financiar tratamentos “sem avaliação de eficácia, segurança, acurácia, efetividade e custo-efetividade”.
 Foto: Lay Amorim/Achei Sudoeste
Foto: Lay Amorim/Achei Sudoeste A Bahia registrou redução do número de casos de arboviroses nas primeiras semanas de de 2026, comparados com os dados obtidos em 2025. De acordo com a Secretária do de Saúde do Estado da Bahia (Sesab), no período de 04 a 19 de janeiro foram registrados 264 casos prováveis de Dengue no estado, diferente dos 1.007 casos notificados em 2025, o que representa uma redução de 73,8%.
Ainda conforme a secretaria, nesse período dois casos foram considerados graves, e nenhum óbito ocorreu. Em relação à chikungunya, o estado contabilizou 18 casos no período avaliado. Correspondendo a uma redução de 84,1% em comparação com o mesmo período de 2024, quando foram registrados 113 casos. O indicador de Zika também indica redução significativa, no início de 2026 nenhum caso foi registrado, contra 36 no ano anterior, uma redução de 100%.
 Foto: Raul Santana/Fiocruz
Foto: Raul Santana/Fiocruz A Secretaria Estadual de Saúde de São Paulo confirmou a morte de um homem por dengue na cidade de Nova Guataporanga, na região Oeste do estado, próxima de Presidente Prudente, área de divisa com o estado do Mato Grosso do Sul. Trata-se da primeira morte pela doença este ano.
Embora os sintomas tenham iniciado no dia 3 de janeiro a data é computada como 2025 para fins epidemiológicos, por ser a semana iniciada no ano passado.
Em 2025, o estado de São Paulo teve 881.280 casos confirmados, 1122 óbitos confirmados e 56 em investigação, além de 1461 casos de dengue grave.
Em 2026, o estado já registra 971 casos confirmados e 3.389 em investigação, dentre os quais dois óbitos. Há até o momento três casos de dengue graves confirmados em território paulista.
As regiões de Araçatuba e Presidente Prudente, no Oeste do estado, têm as maiores taxas de incidência, respectivamente com 13,58 e 8,57 casos por 100 mil habitantes.
Segundo o Ministério da Saúde os casos de dengue no país, em 2026, somam 9.667 casos prováveis com três óbitos em investigação.Em 2025 foram 1.665.793 casos prováveis e 1780 óbitos.
O período de maior incidência da dengue no Brasil nos últimos dois anos foi entre o começo de março (oitava semana) e o final de maio (vigésima semana). As informações são da Agência Brasil.
 Foto: Divulgação/Sesab
Foto: Divulgação/Sesab A Bahia alcançou, em 2025, a marca de 1.384 transplantes de órgãos realizados, número que representa um crescimento de 33% em relação ao ano anterior e consolida o décimo primeiro ano consecutivo de aumento no volume de procedimentos no estado. Os dados foram contabilizados pela Secretaria da Saúde do Estado da Bahia (Sesab), por meio do Sistema Estadual de Transplantes, e refletem o fortalecimento contínuo da política pública de transplantes na rede estadual de saúde.
A secretária da Saúde do Estado, Roberta Santana, comemorou os resultados e destacou o compromisso da gestão com o fortalecimento da política de transplantes na Bahia. “Os números alcançados em 2025 demonstram que estamos no caminho certo. São 11 anos consecutivos de crescimento e um aumento expressivo de 33% no número de transplantes, resultado de investimentos contínuos, do trabalho dedicado das equipes de saúde e do fortalecimento da nossa rede. Cada transplante representa uma nova chance de vida, e seguimos empenhados em ampliar o acesso, reduzir o tempo de espera e incentivar a doação de órgãos em todo o estado”, afirmou a secretária.
Os dados do Sistema Estadual de Transplantes evidenciam a evolução contínua da política de transplantes no estado ao longo da última década. Entre 2015 e 2024, a Bahia saiu de 573 transplantes realizados para 1.040 procedimentos, mais do que dobrando a capacidade transplantadora no período e atingindo 1.384 transplantes realizados em 2025. A série histórica demonstra uma trajetória consistente de crescimento, com destaque para os anos mais recentes, mesmo diante dos impactos da pandemia em 2020.
O coordenador do Sistema Estadual de Transplantes, Eraldo Moura, ressaltou que os resultados refletem o amadurecimento da política de transplantes na Bahia e o esforço contínuo das equipes envolvidas em todo o estado. “O crescimento consistente no número de transplantes é fruto de um trabalho integrado, que envolve desde a identificação do potencial doador até a realização do procedimento. Temos avançado na organização da rede, na capacitação dos profissionais e na melhoria dos fluxos, o que tem permitido salvar cada vez mais vidas. Nosso desafio permanente é ampliar a conscientização das famílias, para que mais doações possam ser efetivadas”, afirmou.
 Foto: Divulgação
Foto: Divulgação A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta segunda-feira, o lenacapavir, primeiro medicamento injetável a cada seis meses que previne a infecção pelo HIV em quase 100%. O fármaco, que será vendido sob o nome comercial de Sunlenca, foi desenvolvido pelo laboratório Gilead Sciences e já havia recebido o aval nos Estados Unidos e na Europa.
O sinal verde da agência reguladora brasileira foi para duas indicações. Uma delas é como profilaxia pré-exposição (PrEP) para prevenir a infecção entre pessoas que não vivem com HIV, tenham idade acima de 12 anos, peso maior que 35 kg e teste negativo para o vírus. A outra é como tratamento de pacientes que vivem com HIV, já tenham utilizado outras terapias e apresentem um quadro de resistência a outras classes de antivirais.
O lenacapavir é considerado inovador por demandar apenas duas aplicações ao ano para garantir uma eficácia de quase 100% contra o HIV. Hoje, já existe uma estratégia de PrEP, disponível inclusive no Sistema Único de Saúde (SUS) desde 2017, mas que envolve comprimidos diários. Eles também reduzem o risco de uma infecção a quase zero, mas o fato de precisarem ser tomados todos os dias é um entrave para a adesão.

Viajar amplia horizontes, estimula a curiosidade e cria lembranças que carregamos por toda a vida. Mas o deslocamento, as mudanças de fuso, a alimentação diferente e a quebra de rotina podem desafiar o corpo e a mente. Quem planeja uma viagem saudável aprende a enxergar descanso, comida e movimento como aliados de cada experiência, e não como obrigações que atrapalham o passeio. A ideia não é seguir regras rígidas, e sim fazer escolhas simples que mantêm o organismo equilibrado. Em voos longos, em ônibus noturnos ou explorando cidades cheias de atrações, pequenas decisões moldam nossa energia e o jeito como apreciamos cada momento. Quando viajamos com atenção ao próprio bem-estar, ficamos menos vulneráveis a indisposições, aproveitamos melhor os dias e voltamos para casa renovados. Juntamente com a equipe da https://jugabet.cl/services/slots, apresentaremos recomendações cientificamente comprovadas, exemplos da vida real e observações práticas que ajudarão você a viajar com tranquilidade, preservando o que mais importa: sua saúde.
Por que o sono é a base de uma boa viagem
O sono atua como um regulador silencioso do corpo. Durante o descanso profundo, o cérebro organiza memórias, o sistema imunológico se fortalece e a musculatura se recupera dos esforços do dia. Em viagens, mudar horários e ambientes interfere nesse processo e pode resultar em cansaço persistente, irritabilidade e menor capacidade de atenção. Ajustar-se gradualmente ao novo fuso horário, sempre que possível, facilita a adaptação do relógio biológico. Criar um ritual simples antes de dormir ajuda o cérebro a reconhecer que é hora de desacelerar, mesmo longe de casa. Reduzir telas e luz intensa nas duas horas anteriores favorece a produção natural de melatonina. Um quarto arejado, escuro e silencioso favorece o descanso, e acessórios como máscara e tampões podem ser úteis quando o ambiente não colabora. Dormir bem não significa passar muitas horas na cama, mas alcançar um sono contínuo e reparador. Viagens com noites mal dormidas tendem a perder brilho, porque tudo exige maior esforço. Já quando priorizamos o descanso, caminhamos mais, observamos melhor e desfrutamos com outra disposição.
Lidar com o jet lag sem perder o ritmo
O jet lag surge quando o relógio interno não acompanha a mudança de fuso. Ele pode provocar sonolência em horários incomuns, dificuldade de dormir, dores de cabeça e queda de desempenho. A adaptação começa antes mesmo de embarcar: aproximar gradualmente os horários de dormir e acordar do fuso de destino facilita o ajuste. Ao chegar, expor-se à luz natural durante o dia ajuda a redefinir o ritmo circadiano, pois o organismo usa a luz como principal sinal para regular hormônios. Manter-se hidratado e fazer refeições leves em horários locais também contribui, permitindo que o corpo “aprenda” a nova rotina. Cochilos curtos podem ser úteis nas primeiras 24 a 48 horas, mas dormir demais durante o dia prolonga o problema. A prática moderada de atividade física, como caminhadas, estimula a circulação e melhora o humor, desde que não seja feita muito perto da hora de dormir. Em poucos dias, a maioria das pessoas se ajusta totalmente e percebe como esse cuidado torna a experiência de viagem mais equilibrada e produtiva.
Alimentação equilibrada fora de casa
Comer bem durante viagens não significa abrir mão dos sabores locais. Trata-se de equilíbrio e de observar como o corpo reage. Refeições muito pesadas, ricas em frituras ou açúcar, geram sonolência e desconforto gastrointestinal, prejudicando passeios e deslocamentos. Preferir alimentos frescos, porções moderadas e incluir frutas, verduras e fontes de proteína favorece a saciedade estável. Em destinos quentes, a perda de líquidos é maior, e beber água com regularidade evita dores de cabeça e queda de energia. Espalhar a ingestão ao longo do dia, sem longos períodos em jejum, mantém o metabolismo ativo. Em mercados locais e feiras é possível encontrar pratos simples e nutritivos, além de conhecer melhor a cultura do lugar. Prestar atenção ao armazenamento e à higiene reduz o risco de infecções alimentares, que são uma das causas mais comuns de mal-estar em viagens. Quando a alimentação apoia o corpo, cada atividade se torna mais prazerosa e o retorno para casa acontece com sensação de bem-estar, não de exaustão.
Manter a hidratação no ritmo certo
A água participa de praticamente todas as funções vitais: regula a temperatura, transporta nutrientes, lubrifica articulações e auxilia na digestão. Em viagens, esquecemos de beber porque a rotina muda, e o acesso nem sempre é fácil. Aviões, por exemplo, possuem umidade muito baixa, o que acelera a desidratação. Carregar uma garrafa reutilizável e enchê-la sempre que possível cria um lembrete constante. Urina muito concentrada e sede intensa são sinais de alerta de que o consumo está insuficiente. Bebidas açucaradas ou muito cafeinadas não substituem a água e podem aumentar a perda de líquidos. Em caminhadas longas ou atividades ao ar livre, ingerir pequenos goles com frequência é melhor do que grandes volumes de uma só vez. O corpo hidratado responde melhor ao calor, mantém a mente mais alerta e reduz a fadiga. Cuidar da hidratação é um gesto simples, mas decisivo para que o viajante se sinta disposto desde a saída até o retorno.
Movimento: como se exercitar sem “quebrar” a viagem
Viajar muitas vezes significa passar horas sentado em transportes e filas. O corpo sente falta de movimento, e músculos e articulações ficam rígidos. Inserir pequenas doses de atividade ao longo do dia previne esse desconforto e melhora o humor. Caminhar é a forma mais acessível e pode ser incorporada aos passeios, permitindo explorar bairros, parques e mirantes. Subir escadas, alongar suavemente após períodos prolongados sentado e fazer breves pausas para circular são atitudes que protegem circulação e postura. Algumas pessoas gostam de levar elásticos de resistência ou usar o peso do próprio corpo para exercícios curtos no quarto do hotel. O objetivo não é bater recordes, e sim manter o organismo ativo. Em vez de encarar o exercício como tarefa, vale enxergá-lo como parte da descoberta do destino. Assim, o movimento vira aliado das experiências, ajudando a dormir melhor, controlar o apetite e aproveitar cada dia com mais leveza.
Prevenindo dores e desconfortos comuns
Viagens longas podem provocar dores lombares, tensão no pescoço e inchaço nas pernas. Ajustar a postura e mudar de posição com frequência reduz esses efeitos. Em ônibus e aviões, apoiar a lombar com uma pequena almofada ou casaco dobrado ajuda a manter o alinhamento da coluna. Alongar panturrilhas e tornozelos estimula o retorno venoso e diminui o risco de inchaço. Carregar mochilas muito pesadas sobre apenas um ombro sobrecarrega músculos e pode causar dor tardia; distribuir melhor o peso é essencial. Outro ponto importante é respeitar sinais do corpo: dor persistente, tontura ou febre merecem atenção e, se necessário, avaliação médica local. Pequenos cuidados evitam que um incômodo se transforme em problema maior e permitem seguir com a programação sem prejuízos. A prevenção, embora discreta, costuma ser o fator que separa uma viagem confortável de uma experiência cansativa.
Saúde mental em trânsito
O bem-estar emocional também viaja conosco. Novos lugares podem gerar entusiasmo, mas também ansiedade e sobrecarga de estímulos. Reservar momentos para pausa ajuda o cérebro a processar tantas novidades. Técnicas simples de respiração e atenção plena reduzem o estresse, especialmente em aeroportos e ambientes lotados. Manter expectativas realistas evita frustrações quando algo foge do planejado, o que é comum em viagens. Dormir, comer e se movimentar com regularidade protege o humor e favorece decisões mais calmas. Quando viajamos com companhia, conversar abertamente sobre preferências e limites previne conflitos. E, sobretudo, lembrar que a viagem não é uma maratona de atrações, mas um encontro com culturas, pessoas e consigo mesmo. Cuidar da mente permite que cada descoberta seja apreciada com presença e curiosidade genuína.
Planejamento que protege a saúde
Planejar com antecedência não elimina imprevistos, mas diminui riscos. Verificar necessidades de vacinação, levar medicamentos de uso contínuo e conhecer os serviços de saúde do destino oferece segurança adicional. Informar-se sobre clima, altitude e costumes locais ajuda o corpo a se adaptar melhor. Documentar alergias e contatos de emergência pode ser decisivo em situações inesperadas. Organizar o itinerário com intervalos razoáveis entre atividades evita sobrecarga e deixa espaço para descanso. Ter um seguro-viagem adequado é outro elemento de proteção, garantindo acesso a cuidados médicos quando necessário. Um planejamento atento funciona como uma rede invisível que sustenta a experiência e permite que o viajante se concentre no que realmente importa: viver momentos significativos com tranquilidade.
Conclusão
Viajar com saúde é um exercício de equilíbrio. Ao cuidar do sono, da alimentação e do movimento, damos ao corpo as condições para responder bem aos desafios do caminho e, ao mesmo tempo, aproveitar intensamente cada experiência. Essas escolhas não exigem perfeição, apenas consciência. Pequenos gestos repetidos ao longo dos dias de viagem se somam e resultam em mais energia, melhor humor e lembranças mais agradáveis. Quando o planejamento inclui o bem-estar, o roteiro ganha profundidade e o retorno para casa acontece com sensação de plenitude. Cada destino oferece oportunidades únicas, e estar fisicamente e emocionalmente preparado é a melhor forma de honrar essas oportunidades. Assim, toda viagem se transforma não só em descoberta do mundo, mas também em um aprendizado sobre como cuidar de si em qualquer lugar.
 Foto: Marcelo Camargo/Agência Brasil
Foto: Marcelo Camargo/Agência Brasil O governo federal vai construir o primeiro hospital público inteligente do Brasil na cidade de São Paulo. Os recursos virão do empréstimo de R$ 1,7 bilhão do Novo Banco de Desenvolvimento (NDB), o banco do Brics. O anúncio foi feito nesta quarta-feira (7) em cerimônia no Palácio do Planalto com a presença do presidente Luiz Inácio Lula da Silva, do ministro da Saúde, Alexandre Padilha e da presidenta do NDB, Dilma Rousseff.
Segundo o Ministério da Saúde, o hospital será referência nacional e modelo de assistência em saúde totalmente digital para os países do bloco. A unidade atenderá os pacientes da rede pública com medicina de alta precisão, apoiada por inteligência artificial e outras tecnologias emergentes. Integrará, também, a rede de hospitais e serviços inteligentes com 14 unidades de terapia intensiva (UTIs) automatizadas, que funcionarão de forma interligada em diversos estados.
A modernização de hospitais de excelência do Sistema Único de Saúde (SUS) também faz parte do projeto.
O novo hospital vinculado à Universidade de São Paulo (USP) terá um setor de emergência com 250 leitos e capacidade para atender 200 mil pacientes por ano. A Unidade de Terapia Intensiva (UTI) contará com 350 leitos conectada com as UTIs inteligentes. Haverá 25 salas para cirurgia. A previsão para que a unidade fique pronta é de três a quatro anos.
Os serviços inteligentes de saúde usam infraestrutura com tecnologias digitais para otimizar processos e melhorar os resultados para os pacientes. Segundo o ministério, o primeiro hospital inteligente poderá reduzir em mais de cinco vezes o tempo de espera por atendimento especializado em situações de urgência e emergência.
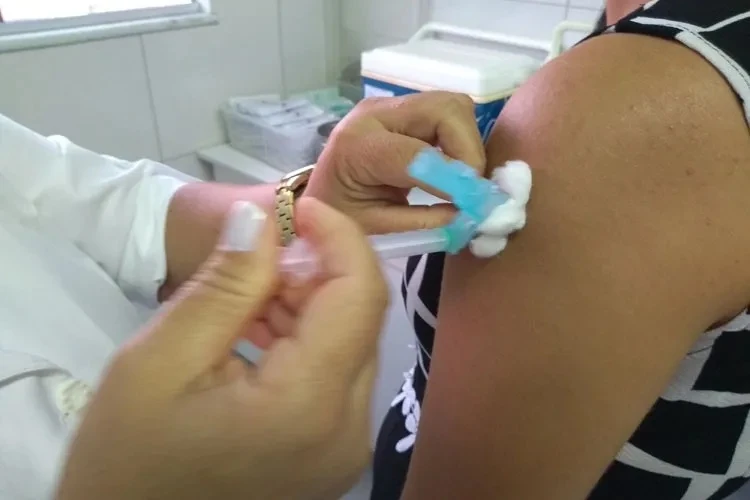 Foto: Lay Amorim/Achei Sudoeste
Foto: Lay Amorim/Achei Sudoeste Os jovens brasileiros de 15 a 19 anos que não receberam a vacina contra o HPV na idade recomendada têm até o primeiro semestre de 2026 para se vacinarem, por meio da estratégia de resgate vacinal do Ministério da Saúde. A estimativa é vacinar 7 milhões de jovens nessa faixa etária.
Até dezembro de 2025, foram aplicadas 208,7 mil doses da vacina no âmbito da estratégia de resgate, sendo 91 mil em meninas e 117,7 mil em meninos. Além de estar disponível nas Unidades Básicas de Saúde (UBS) a vacinação também é realizada por meio de ações em escolas, universidades, ginásios esportivos e shoppings.
O Ministério da Saúde classifica o HPV (Papilomavírus Humano) como o vírus que afeta a pele e as mucosas, sendo a infecção sexualmente transmissível mais comum no mundo. Existem mais de 200 tipos de HPV, alguns dos quais podem causar verrugas genitais, enquanto outros estão associados a tumores malignos, como o câncer do colo do útero, ânus, pênis, boca e garganta.
Desde 2024, o Brasil adotou o esquema de dose única da vacina, substituindo o modelo anterior de duas doses e simplificando o acesso à imunização. Para pessoas imunocomprometidas, como aquelas que vivem com HIV/Aids, pacientes oncológicos e transplantados, o esquema vacinal permanece com três doses. A mesma recomendação se aplica a usuários de PrEP entre 15 e 45 anos e a vítimas de violência sexual a partir dos 15 anos.
 Foto: Fernando Frazão/Agência Brasil
Foto: Fernando Frazão/Agência Brasil O estado de São Paulo registrou o segundo caso de sarampo este ano. Segundo a Secretaria Estadual da Saúde, o paciente é um homem de 27 anos, morador da capital paulista, não vacinado e que havia viajado recentemente ao exterior. Segundo a pasta, ele já recebeu atendimento médico e teve alta.
O outro caso havia sido identificado em abril deste ano, também em um morador da capital paulista.
Entre janeiro e novembro deste ano, 37 casos de sarampo foram confirmados em todo o Brasil, segundo informações do Ministério da Saúde. Todos estes casos foram importados, ou seja, adquiridos em viagens, sem transmissão local do vírus.
O número de casos de sarampo vem se intensificando neste ano na região das Américas. Até o dia 7 de novembro de 2025, segundo a Organização Pan-Americana da Saúde (Opas), foram confirmados 12.596 casos de sarampo em dez países das Américas, com 28 óbitos, a maior parte deles registrados no México.
De acordo com a Opas, essa transmissão tem afetado principalmente comunidades com baixa cobertura vacinal: 89% dos casos ocorreram em pessoas não vacinadas ou com status vacinal desconhecido.
 Foto: Tetra Images/Getty Images
Foto: Tetra Images/Getty Images Quase metade das crianças brasileiras demonstra algum nível de ansiedade, irritabilidade ou inquietação associado ao uso de telas. O dado faz parte de uma pesquisa inédita do Projeto Brief sobre adultização e uso precoce das redes sociais no país.
O estudo ouviu 1.800 pais sobre o apoio à regulamentação das redes para assegurar um ambiente digital seguro para crianças e adolescentes. O estudo revela um cenário crescente de preocupação entre as famílias: 46% das crianças apresentam comportamentos negativos relacionados ao tempo diante de celulares, tablets, computadores e televisores.
Segundo o levantamento, a ansiedade é o sintoma mais frequente, citado por 27% dos responsáveis. Outros efeitos destacados são irritabilidade (25%), dificuldade de concentração (23%) e alterações no sono (20%). Entre os cuidadores entrevistados, 70% afirmam que gostariam de reduzir o tempo de tela dos filhos, mas têm dificuldade em ajustar a rotina, especialmente diante da sobrecarga de trabalho, da falta de espaços de lazer e do apelo constante das plataformas digitais.
A pesquisa também aponta que 60% das crianças utilizam telas para entretenimento entre uma e três horas por dia. Ou seja, acima do recomendado por especialistas em desenvolvimento infantil. Para crianças com menos de até 5 anos, a Sociedade Brasileira de Pediatria (SBP) orienta um uso bastante restrito e sempre supervisionado; mesmo assim, entre os entrevistados, 30% das crianças nessa faixa etária passam mais de duas horas diárias conectadas.
O impacto no comportamento preocupa. Responsáveis relatam que, ao retirar o acesso digital, 44% das crianças apresentam resistência intensa, como choro, frustração exagerada ou reações agressivas. O estudo ainda mostra que 52% das famílias percebem piora na convivência doméstica quando o uso de telas aumenta, principalmente em períodos sem escola ou feriados prolongados.
Para especialistas ouvidos pelo levantamento, o excesso de tempo online afeta habilidades essenciais do desenvolvimento, como interação social, autorregulação emocional e brincadeira livre — etapa considerada fundamental na primeira infância. Eles alertam para a necessidade de que a mediação adulta seja ativa, com regras claras, diálogo e estímulo a atividades fora do ambiente digital.
A pesquisa também investigou a percepção dos adultos sobre a própria relação com as telas. Mais da metade (56%) admite que o próprio uso de celular interfere no tempo de qualidade com os filhos, criando um ciclo em que adultos e crianças reproduzem comportamentos semelhantes.
Os dados reforçam um debate urgente: como equilibrar tecnologia e infância em um país onde a conectividade é parte central da vida cotidiana? Para os especialistas, o ponto não é proibir o acesso, mas construir hábitos saudáveis que priorizem o brincar, o descanso, a convivência e a segurança emocional.
 Foto: Joédson Alves/Agência Brasil
Foto: Joédson Alves/Agência Brasil O Brasil foi reconhecido pela Organização Mundial de Saúde (OMS) como o maior país do mundo a eliminar a transmissão do HIV de mãe para filho, a chamada transmissão vertical, como problema de saúde pública. O ministro da Saúde, Alexandre Padilha, antecipou o anúncio durante o programa Bom Dia, Ministro, do CanalGov, na sexta-feira (15).
Segundo Padilha, o Conselho da Unaids (Programa Conjunto das Nações Unidas sobre HIV/AIDS) em conjunto com representantes da OMS visitará o Brasil esta semana para a entrega oficial da certificação ao governo brasileiro.
“Significa que o Brasil conseguiu eliminar graças ao SUS [Sistema Único de Saúde], aos testes rápidos das unidades básicas de saúde, aos testes do pré-natal, às gestantes que têm HIV tomarem a medicação pelo SUS”, disse Padilha.
O ministro lembrou que há algumas décadas o Brasil tinha iniciativas filantrópicas para manutenção de abrigos para órfãos com HIV, que haviam perdido os pais em decorrência da Aids.
“Abrigavam aqueles bebês que tinham nascido com HIV e seus pais tinham morrido. A gente não tem mais isso no nosso país, felizmente, nem a transmissão do HIV da gestante para o bebê”, comemorou.
Segundo o ministro, o Brasil apresentou um dossiê à organização mundial no mês julho com os dados do SUS no Brasil.
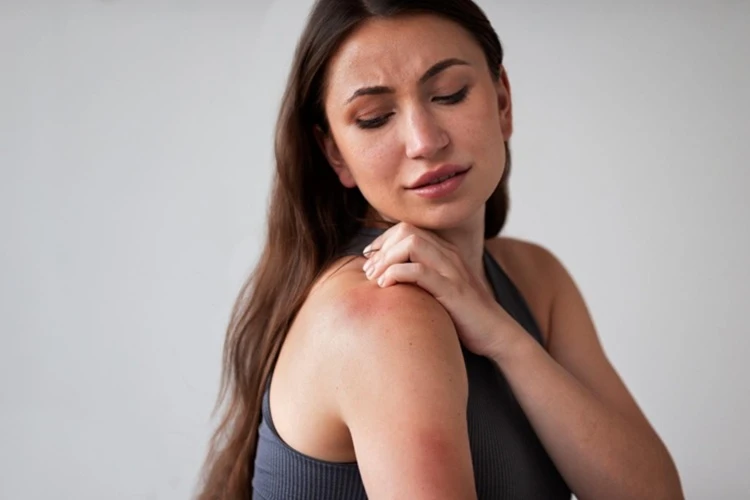 Foto: Freepik
Foto: Freepik Pele seca, coceira incessante e manchas vermelhas transformam a rotina de milhões de brasileiros em um verdadeiro desafio. A dermatite atópica, conhecida também como eczema, é uma doença inflamatória crônica que surge tanto em crianças quanto em adultos, seguindo um curso imprevisível de crises e melhoras.
Os números impressionam: a cada ano, esse diagnóstico atinge até um quarto das crianças e 10% da população adulta. Não é por acaso que os consultórios dermatológicos têm ficado cada vez mais cheios.
A busca por um especialista qualificado virou prioridade para milhares de brasileiros. Plataformas como a AvaliaMed registram um aumento significativo do termo de busca dermatologista perto de mim em São Paulo, ou em outra região, um sinal claro da necessidade de encontrar alívio e tratamento adequado para uma condição que exige atenção constante.
Entendendo a raiz do problema
De fundo hereditário e crônico, ela não passa de uma pessoa para outra. A medicina ainda busca respostas sobre sua causa exata, mas já se sabe que ela frequentemente anda de mãos dadas com outras alergias familiares, como asma e rinite – uma combinação conhecida como "tríade atópica".
Tudo começa com uma falha genética na barreira que protege nossa pele. Imagine uma parede de tijolos onde o cimento está faltando. É mais ou menos isso que acontece: a pele, sem sua proteção natural, fica frágil, permitindo que a água escape e que irritantes e alérgenos invadam com facilidade, desencadeando a inflamação.
A vida com dermatite atópica é marcada por altos e baixos. As crises surgem de forma cíclica, sem aviso, e são provocadas por uma série de fatores do dia a dia. "Gatilhos ambientais comuns incluem banho em excesso, sabões abrasivos, presença da bactéria Staphylococcus aureus na pele, sudorese e tecidos grosseiros como a lã", de acordo com o manual médico MSD.
O estresse emocional e mudanças bruscas de temperatura também são fatores agravantes conhecidos.
Os sinais que a pele mostra
Reconhecer a dermatite atópica é observar uma história que se desenha na pele, variando com a idade e a fase da doença. A coceira intensa é, sem dúvida, a personagem principal desse drama. Um prurido tão severo que cria um círculo vicioso: coça-se para aliviar, mas o ato de coçar agride ainda mais a pele, piora a inflamação e pode abrir feridas, causar sangramentos e facilitar infecções. O alívio momentâneo cobra um preço alto.
Além da coceira insuportável, a pele apresenta suas queixas de forma visível. Ressecada por natureza, nela podem aparecer pequenas elevações, bolhinhas, vermelhidão, inchaço e descamação. Quando o ato de coçar vira um hábito crônico, a pele se defende: ela engrossa, escurece e forma sulcos, um fenômeno chamado liquenificação, que é a marca registrada de um problema de longa data.
Onde essas lesões aparecem também conta uma história. Nos bebês e nas crianças pequenas, o rosto, o couro cabeludo, as mãos, os braços, os pés e as pernas são os palcos mais comuns.
Conforme os anos passam, o cenário muda. Em crianças maiores e adultos, o eczema prefere se instalar nas dobras do corpo – à frente dos cotovelos, na parte de trás dos joelhos, o pescoço e, por vezes, as mãos e os pés.
Mapeando as possibilidades de tratamento
Segundo os especialistas da área, controlar a dermatite atópica é uma missão personalizada. O objetivo é domar os sintomas, acalmar a inflamação e evitar que novas crises surjam. A cura definitiva ainda não existe, mas uma vida plena e com a pele sob controle é perfeitamente possível.
A base de tudo, o alicerce que não pode ser ignorado, é a hidratação intensiva e diária. Usar cremes específicos, os emolientes, sem perfume e ricos em óleos, é como reconstruir o "cimento" faltante na barreira da pele. Aplicá-los logo após o banho, com a pele ainda úmida, é um truque valioso para selar a hidratação e ajudar na reparação. É um cuidado básico, porém transformador.
Quando a crise vem, com sua vermelhidão e coceira, entram em cena os medicamentos tópicos. Cremes e pomadas de corticosteroides ou inibidores de calcineurina são os grandes aliados para apagar o incêndio inflamatório. Assim, seguir à risca a orientação médica sobre a potência e o tempo de uso é crucial para o sucesso.
Para os casos mais rebeldes, que resistem aos tratamentos aplicados na pele, é preciso partir para opções sistêmicas. Remédios orais, como anti-histamínicos para a coceira noturna ou imunossupressores, podem ser necessários.
De fato, nos últimos anos, a medicina deu um salto com os chamados biológicos, como o dupilumabe, uma medicação inteligente que mira especificamente os mecanismos da inflamação. Para alguns pacientes, a fototerapia – tratamento com luz ultravioleta em ambiente controlado – também se mostra uma alternativa eficaz.
 Foto: Reprodução/TV Brasil
Foto: Reprodução/TV Brasil A Agência Nacional de Vigilância Sanitária (Anvisa) publicou nesta segunda-feira (8) no Diário Oficial da União (DOU) o registro da vacina contra a dengue desenvolvida pelo Instituto Butantan.
O registro do imunizante já havia sido anunciado pelo ministro da Saúde, Alexandre Padilha, no fim de novembro. A intenção da pasta é começar a aplicação das doses em 2026, de forma gratuita, via Sistema Único de Saúde (SUS).
Em nota, a Anvisa informou que a publicação oficializa a conclusão do processo regulatório e permite a produção e a comercialização do imunizante — que será ofertado exclusivamente pela rede pública.
“O registro é um marco para o enfrentamento da dengue no Brasil. A vacina passou por todas as etapas de análise técnica e regulatória previstas na legislação sanitária, garantindo sua segurança, qualidade e eficácia”, destacou a agência.
O comunicado cita ainda que a vacina é tetravalente e combate os quatro sorotipos da dengue, além de ser aplicada em dose única. “Essa é a primeira vacina contra a dengue a ser produzida por um laboratório nacional”, completou a Anvisa.
A nota ressalta que, mesmo com o registro do imunizante, o Instituto Butantan deve dar continuidade aos estudos adicionais da vacina e realizar o monitoramento ativo de seu uso pela população em geral.
“A tecnologia utilizada pelo novo imunizante é a de vírus vivo atenuado, que é segura e já empregada em diversas outras vacinas em uso no Brasil e no mundo”, destacou a agência.
A indicação da dose aprovada pela Anvisa é para pessoas na faixa etária de 12 a 59 anos, perfil que, segundo a nota, ainda pode ser ampliado no futuro, a depender de novos estudos.
Em novembro, o Instituto Butantan informou que já havia 1 milhão de unidades da vacina prontas para distribuição. A estimativa do Butantan é ter disponível mais de 30 milhões de doses em meados de 2026.
 Foto: João Risi/MS
Foto: João Risi/MS O Ministério da Saúde inicia, nesta terça-feira (2), a distribuição nacional da vacina contra o vírus sincicial respiratório (VSR). O primeiro lote, com 673 mil doses, será enviado a todos os estados e ao Distrito Federal. A imunização, ofertada gratuitamente pelo SUS, é destinada a gestantes a partir da 28ª semana e tem como objetivo reduzir casos de bronquiolite em recém-nascidos. Com a chegada das doses, estados e municípios poderão iniciar imediatamente a vacinação nos postos de saúde.
“Esse é mais um passo decisivo para proteger gestantes e recém-nascidos de uma das infecções respiratórias mais graves do período neonatal. A chegada dessa vacina é uma novidade e reforça o compromisso do SUS com a prevenção e com o cuidado integral das famílias brasileiras”, afirmou o ministro da Saúde, Alexandre Padilha.
O lote inicial integra a compra de 1,8 milhão de doses feita pela pasta. As entregas seguem calendário pactuado com estados e municípios. O DF é a primeira unidade da federação a receber as doses. Os demais estados recebem entre os dias 2 e 3 de dezembro. As entregas são feitas por modal aéreo, rodoviário e multimodal, seguindo logísticas de cada estado. O Ministério da Saúde vai garantir o abastecimento necessário para a execução das estratégias locais de vacinação.
A oferta da vacina no SUS, que na rede privada pode custar até R$ 1,5 mil, foi viabilizada por meio de acordo entre o Instituto Butantan e o laboratório produtor, que assegurou a transferência de tecnologia ao Brasil. Com isso, o país passará a fabricar o imunizante, ampliando autonomia e acesso da população a essa proteção.
 Foto: Marcelo Camargo/Agência Brasil
Foto: Marcelo Camargo/Agência Brasil O ministro da Saúde, Alexandre Padilha, anunciou nesta quarta-feira (26) o registro pela Agência Nacional de Vigilância Sanitária (Anvisa) da vacina da dengue (Butantan-DV) produzida pelo Instituto Butantan. A intenção é começar a aplicação das doses em 2026, de forma gratuita, pelo Sistema Único de Saúde (SUS).
Segundo o Instituto Butantan, já há 1 milhão de unidades da vacina contra a dengue prontas para distribuição. Este é o primeiro imunizante no mundo de apenas uma dose. A estimativa do Butantan é ter disponível mais de 30 milhões de doses em meados de 2026.
“Hoje é um dia de alegria, de vitória da vacina, de vitória da ciência, de vitória da cooperação entre o SUS brasileiro e de suas instituições públicas que estão espalhadas pelo país, entre elas o Instituto Butantan”.
Padilha, ao lado do governador de São Paulo, Tarcísio de Freitas, ressaltou a qualidade da vacina contra a dengue.
“Sabemos já dos dados publicados, sabemos da segurança dessa vacina. Estamos falando de um hat-trick: é uma vacina 100% brasileira, tem capacidade de proteção ampla e é uma dose apenas”.
A nova vacina será integrada ao Programa Nacional de Imunização (PNI). De acordo com o governo, o ministério apresentará a novidade já nesta quinta-feira (27) à Comissão Tripartite, formada por secretários estaduais e municipais de saúde, bem como a estratégia de incorporação.
“Queremos começar a utilização dessa vacina no começo do calendário vacinal de 2026”, revelou o ministro.
 Foto: Ricardo Stuckert/PR
Foto: Ricardo Stuckert/PR O ministro da Saúde, Alexandre Padilha, esteve nesta segunda-feira (17) em Guarulhos (SP) para receber o primeiro lote com mais de dois milhões de unidades de insulina glargina, que atende os portadores de diabetes tipo 2.
“Hoje é um grande dia para o SUS [Sistema Único de Saúde], um grande dia para a soberania da saúde no Brasil e um grande dia para a segurança dos pacientes que têm diabetes tipo 2”, disse o ministro em coletiva no Aeroporto de Guarulhos.
Já oferecido para quem tem o tipo 1 da doença, o produto foi adquirido através de Parceria para o Desenvolvimento Produtivo (PDP) e haverá transferência de tecnologia para o laboratório público Bio-Manguinhos (Fiocruz).
Assim, o medicamento passará a ser produzido no país, o que fará com que o Brasil deixe de depender do mercado externo.
“É uma segurança, porque faz com que esse paciente não fique submetido a crises internacionais da insulina, como existem hoje”, afirmou o ministro.
Para Padilha, o tratamento com a insulina glargina é um grande avanço: "Ela é de uso mais fácil e a resposta também é melhor”.
A produção do medicamento no Brasil será feita pela Friocruz junto com a Biomm em uma parceria com a chinesa Gan&Lee, uma das maiores produtoras mundiais de insulina.
“É uma parceria que acontece por conta do fortalecimento do SUS, da decisão do Ministério da Saúde junto com estados e municípios de passar a ofertar insulina glargina também para quem tem diabetes tipo 2”, explica Padilha.
A expectativa, de acordo com o ministro, é de que com a transferência de tecnologia para a Fiocruz, a produção – no estado do Ceará – chegue a algo em torno de 30 a 40 milhões de unidades por ano.
“É uma grande parceria que traz garantia e segurança para os pacientes brasileiros”.
Atualmente, cerca de 20 milhões de pessoas têm diabetes no país.
Segundo o ministro, além deste carregamento, o Brasil ainda vai receber mais 4,7 milhões de unidades até o final do ano, chegando a quase sete milhões. Assim, o investimento do governo federal no combate ao diabetes, em 2025, será de R$ 131,8 milhões.
 Foto: Tânia Rêgo/Agência Brasil
Foto: Tânia Rêgo/Agência Brasil A vacina contra a dengue produzida pelo Instituto Butantan pode ser aprovada a partir do final da semana que vem pela Agência Nacional de Vigilância Sanitária (Anvisa). O anúncio foi feito na sexta-feira (7), em coletiva de imprensa que tratou sobre a necessidade de acelerar as filas para aprovação de medicamentos sintéticos e produtos biológicos.
“A vacina de dengue do Butantan é um processo prioritário para a agência”, afirmou o diretor da Anvisa Daniel Pereira. Ele explicou que, na semana passada, houve uma reunião com o comitê de especialistas para suprir dúvidas que ficaram em relação à vacina. “A nossa expectativa é que, na primeira quinzena de novembro ainda, ou alguns dias a mais, a gente já tenha uma conclusão por parte da Anvisa, para a gente autorizar o registro”, explicou.
Pereira acrescentou que essa análise demandou “muitas horas” de discussão técnica com especialistas externos que apoiaram a decisão. Segundo a Anvisa, não houve solicitações de registro de outros imunizantes por parte dos demais laboratórios.
 Foto: Marcelo Camargo/Agência Brasil
Foto: Marcelo Camargo/Agência Brasil A Agência Nacional de Vigilância Sanitária (Anvisa) proibiu a comercialização, distribuição, fabricação, propaganda e uso de todos os suplementos alimentares e energéticos da empresa OZT Comércio Atacadista Especializado em Produtos Ozonizados.
Também foi determinada a apreensão dos produtos, que têm adição de ozônio, um tipo de gás que não tem avaliação de segurança para uso como parte de suplementos alimentares e composto líquido pronto para o consumo, como energéticos.
Atualmente, a autorização para uso de ozônio é apenas como agente de desinfecção no tratamento de água.
Segundo a agência, a empresa divulgou propagandas desses alimentos com indicações terapêuticas e alegações funcionais e de saúde não aprovadas, como a alegação de que o produto “oferece suporte nutricional para o funcionamento saudável do sistema digestivo, hepático, ocular e cardiovascular”.
A Anvisa esclarece que as autorizações para suplementos alimentares estão relacionadas a papéis metabólicos dos nutrientes ou substâncias no organismo, quando consumidos como parte de uma dieta. “Nenhuma das alegações aprovadas para alimentos está associada com finalidades medicamentosas ou terapêuticas, que são exclusivas de medicamentos e devem ser comprovadas cientificamente”, explica a agência, em nota.
 Foto: Raul Santana/Fiocruz
Foto: Raul Santana/Fiocruz O Ministério da Saúde vai promover uma ação de mobilização nacional contra a dengue no próximo sábado (8). O objetivo é conscientizar gestores públicos, profissionais da saúde e a população em geral sobre a importância das medidas recomendadas para conter a proliferação do mosquito Aedes aegypti, principal transmissor da doença.
“A gente age ao longo de todo o ano, mas agora é a oportunidade de voltarmos a chamar a atenção da população para evitarmos qualquer tipo de cenário, de crescimento do número de casos”, declarou o ministro da Saúde, Alexandre Padilha, ao anunciar a realização do Dia D contra a dengue. A iniciativa faz parte da campanha nacional “Não Dê Chance para Dengue, Zika e Chikungunya”, que o ministério lançou nesta segunda-feira (3).
“Agora é hora de organizar a assistência à saúde, reforçar as ações de prevenção e orientação e identificar os pontos estratégicos a atacar nas cidades”, acrescentou o ministro.
De acordo com o ministério, em 2025, foram registrados, até o momento, 1.611.826 casos prováveis de dengue e 1.688 mortes. Ainda segundo a pasta, os resultados são, respectivamente, 75% e 72% inferiores aos do mesmo período de 2024.

