Foto: Freepik
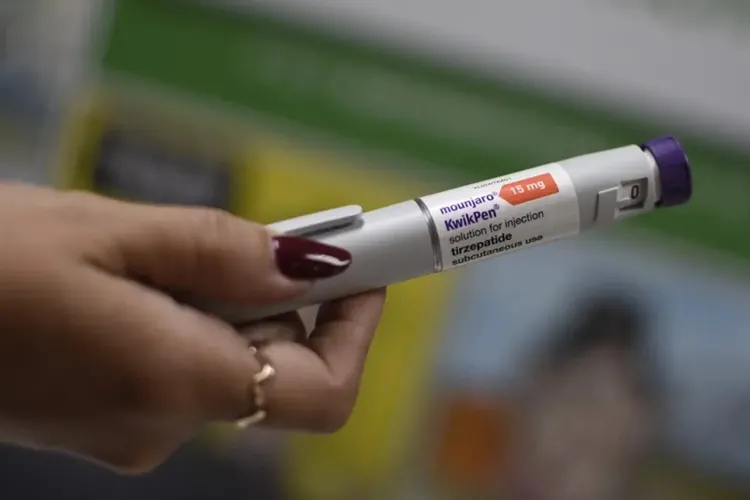
Foto: Freepik A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o uso de Mounjaro (tirzepatida) para o tratamento do diabetes tipo 2 em crianças e adolescentes de 10 a 17 anos no Brasil. O medicamento, da farmacêutica Eli Lilly, é o primeiro do grupo de agonistas duplos dos receptores GIP/GLP-1 a ser liberado para essa faixa etária no país. A aprovação ocorreu nesta quarta-feira (22).
A agência aprovou o medicamento após resultados de fase 3 do estudo clínico internacional SURPASS-PEDS, que indicaram uma remissão glicêmica de até 4 entre 5 pacientes. Houve redução superior a 2 pontos percentuais na hemoglobina glicada e queda de até 12% no IMC (Índice de Massa Corporal).
No Brasil, existem cerca de 213 mil adolescentes vivendo com diabetes tipo 2. O país atualmente figura entre as nações com maior número de pacientes na faixa pediátrica vivendo com a condição. Com a nova opção de tratamento, há chances de regressão nos casos da doença.
“A aprovação de Mounjaro para pacientes pediátricos com diabetes tipo 2 representa mais um avanço da ciência com impacto social”, afirmou Luiz André Magno, diretor médico sênior da Lilly, em comunicado enviado à CNN Brasil.
“Crianças e adolescentes com essa condição enfrentam uma doença de progressão mais veloz do que em adultos, e as opções disponíveis até hoje frequentemente apresentavam limitações para controlar adequadamente os níveis glicêmicos. Mounjaro chega como uma resposta inovadora, com eficácia robusta e perfil de segurança bem estabelecido, para transformar a jornada do cuidado dessa população, que por conceito, é mais vulnerável”, assegurou.